В этой статье рассмотрим понятия «дым» и «аэрозоль». Выясним, какое отношение они имеют к кальяну, а также разберем физические показатели кальянного «дыма» в сравнении с сигаретным, вейперским и аэрозолем систем нагревания табака (на примере Iqos’а).
Начнем с определения дыма.
Дым – аэрозоль, состоящий из мелких твердых частиц и образующийся при сгорании чего-либо.
Из него вытекают три важные мысли: первая – дым является аэрозолем; вторая — источником образования дыма является реакция горения; третья – частицы дыма должны содержать твердые вещества. Для уточнения приведем определение аэрозоля:
Аэрозоль – дисперсная система, состоящая из взвешенных в газовой среде (в большинстве случаях окружающем нас воздухе), мелких твердых или жидких частиц.
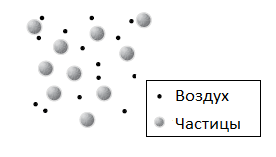
Теперь попробуем применить оба определения к кальяну.
Чтобы вдыхаемое «облако» назвать дымом, надо обнаружить процесс горения и наличие твердых частиц. Аэрозолем его назвать можем всегда, так как это общее понятие. На текущий момент нет научных подтверждений, что в кальянном аэрозоле содержатся твердые частицы, потому что никто не проводил подобного исследования. Наличие реакции горения или её отсутствия в чаше сейчас рассматривать не будем. Эту тему лучше раскрыть в отдельной статье. Да и на самом деле процессы в чаше нам сейчас не столь важны, так как есть куда более очевидный момент. Связан он с углем. Уголь в процессе курения горит. Это неоспоримый факт.
За счет этого процесса уголь выделяет в аэрозоль твердые продукты горения. В литературе определены физические и химические показатели этих частиц [1,10,11]. Поэтому без постановки эксперимента по нахождению твердых частиц в кальянном аэрозоле мы можем точно сказать, что это дым. Но есть интересный момент, который стоит оговорить.
Если заменить уголь на любую электрическую систему нагрева чаши, то наличие реакций горения в cистеме становится не очевидным и в таком случае кальянный аэрозоль дымом назвать будет не верно без должной аргументации. Данный факт можно было бы использовать для легальных обходов действующих антитабачных законодательств. Единственное для большей авторитетности потребовалось бы все-таки провести исследование на наличие твердых частиц в кальянном аэрозоле при использовании угля и его электронного аналога. Необходимые исследования проводились при выходе на рынок систем нагревания табака (Iqos [2], к примеру).
Ключевой вывод из этих рассуждений – чтобы понять физику курения кальяна, нам необходимо изучить основы физики аэрозолей. Начнем со способов образования аэрозолей.
Способы образования аэрозолей
Существует два основных способа образования аэрозолей — диспергационный (от большого к малому) и конденсационный (от малого к большому).
Диспергационные аэрозоли (аэрозоли измельчения) – это аэрозоли, образующиеся вследствие измельчения твердых и жидких веществ.
Подобные аэрозоли образуются [3]:
- -при разбрызгивании жидкостей (водяные туманы в водопадах, аэрозоли из слизи, образующиеся -при кашле и чихании, аэрозоли, получаемые с помощью аэрозольных баллончиков и т.д.);
- -при измельчении твердых тел и взмучивания порошков (пыль при подметании и пересыпании муки, при разрушении каменных стен и т.д.);
Данный способ не имеет отношения ни к кальянным смесям, ни к другим табачным продуктам.

Аэрозоли конденсации (охлаждения) – это аэрозоли, которые образуются вследствие охлаждения и образования пересыщенного пара, частицы которого хорошо конденсируются на ядрах конденсации (мельчайших твердых или жидких частицах, газовых ионах, находящихся в воздухе), а также в результате химических реакций между двумя или несколькими веществами (если образуется новое вещество с меньшей летучестью).

Ключевой термин в этом определении пересыщенный пар. Такое состояние пара является метастабильным, то есть пар способен существовать длительное время в нем, однако оно является термодинамически неустойчивым. При появлении ядер конденсации часть пара конденсируется на них, давление оставшегося пара падает, и он переходит в устойчивое состояние насыщенного пара. Устанавливается динамическое равновесие между жидкостью и газом. Пересыщенный пар может быть получен путём увеличения давления пара в объёме, свободном от ядер конденсации (пылинок, ионов, капелек жидкости малых размеров и т. д). Другой способ получения — охлаждение пара, который находится в равновесии со своей жидкостью или твердым телом, при тех же условиях.
Объемная конденсация пересыщенного пара и приводит к образованию частиц аэрозоля. Это может происходить в трех случаях:
1) при адиабатическом расширении;
2) при смешении паров и газов, имеющих разные температуры;
3) при охлаждении газовой смеси.
1. Адиабатическое расширение газа.
Таким путем образуются облака. Теплые массы влажного воздуха поднимаются в верхние слои атмосферы. Так как c увеличением высоты атмосферное давление падает, происходит адиабатическое расширение (без подвода тепла), которое сопровождается охлаждением воздуха и конденсацией водяного пара. На относительно небольшой высоте образуются кучевые облака, в которых вода находится в виде жидких капель, в верхних же слоях атмосферы, где температура более низкая, возникают перистые облака, содержащие кристаллики льда.
2. Смешение газов и паров, имеющих разные температуры.
Так образуются атмосферные туманы. Чаще всего туман появляется при ясной погоде ночью, когда теплая поверхность Земли сильно охлаждается. Теплый влажный воздух соприкасается с охлаждающейся Землей или с холодным воздухом вблизи ее поверхности и в нем образуются капельки жидкости. То же происходит при смешении фронтов теплого и холодного воздуха.
3. Охлаждение газовой смеси, содержащей пар.
Этот случай разберем на примере чайника, в котором закипела вода. Из носика выходит водяной пар, который невидим, поскольку не рассеивает свет. Далее водяной пар быстро охлаждается, вода в нем конденсируется, и уже на небольшом расстоянии от носика чайника появляется туман, ставший видимым из-за способности рассеивать свет. Аналогичное явление наблюдается, когда открыта форточка в морозный день. Более прочный аэрозоль образуется, когда на сковородке кипит масло и создает в помещении масляный аэрозоль.
Аэрозоли всех курительных табачных продуктов образуются конденсационным способом. Остановимся более подробно на физике аэрозолей.
Физика аэрозолей
Особенности физических свойств аэрозолей обусловлены:
• малой концентрацией частиц — так, если в 1 см3 гидрозоля золота содержится 1016 частиц, то в таком же объеме аэрозоля золота менее 107 частиц;
• малой вязкостью воздуха, следовательно, малым коэффициентом трения, возникающего при движении частиц;
• малой плотностью дисперсионной среды (ρчаст » ρвоздуха).
Все это приводит к тому, что движение частиц в аэрозолях происходит значительно интенсивнее, чем лиозолях (где частицы распределены в жидкости). В отличие от остальных дисперсных систем (гели, пены, эмульсии и т.д.) в аэрозолях отсутствует всякое взаимодействие между поверхностью частиц и газовой средой, а значит, отсутствуют силы, препятствующие сцеплению частиц между собой и с макроскопическими телами при соударении. Поэтому аэрозоли являются агрегативно неустойчивыми системами, т.е. каждое столкновение частиц приводит к их слипанию. Независимо от начальной концентрации аэрозоля через несколько минут в 1 см3 находится 108-106 частиц (для сравнения — в лиозолях ~ 1015 частиц). Стоит добавить, что частицы составляют очень малую долю, менее 0,0001%, от общей массы или объема аэрозоля. Таким образом, аэрозоли — это очень разбавленные системы. При этом газовая среда в основном влияет на поток частиц под действием гидродинамических сил.
Рассмотрим более подробно какие процессы могут протекать с частицей аэрозоля. На рис. 4 показаны ключевые из них.
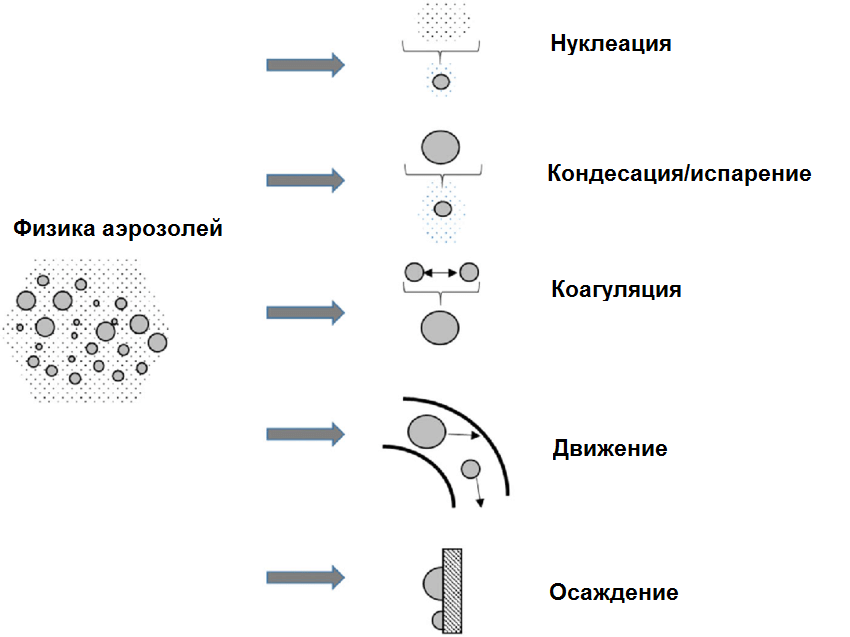
Нуклеация – это процесс образования частиц аэрозоля из конденсировавшегося пересыщенного пара. Для понимания, как это происходит вспомним два термина из школьного курса физика – парциальное давление и давление насыщенного пара.
Парциальное давление пара — давление, которое пар мог бы оказывать, если бы он был единственным присутствующим компонентом в смеси.
Это давление, выраженное в виде доли давления окружающей среды, является фракционной концентрацией пара. Воздух при 20 0С и относительной влажности 50% имеет парциальное давление водяного пара 1,17 Па, что означает, что водовоздушная смесь по объему содержит 1,17/101 = 1,2% водяного пара.
Давление насыщенного пара — давление пара, при котором жидкость находится в равновесии со своим паром.
Давление насыщенных паров является уникальным свойством любой жидкости при заданной температуре. Оно представляет собой минимальное парциальное давление паров жидкости, которое должно поддерживаться на границе раздела газ-жидкость для предотвращения испарения. Этот термин применим для плоской поверхности жидкости.
Коэффициент насыщения SR — соотношение парциального давления пара и давления насыщенных паров.
Когда SR равно единице, пар является насыщенным, когда SR больше единицы, пар пересыщен, а когда меньше единицы, он ненасыщен. Поскольку аэрозольные частицы имеют изогнутую поверхность, для поддержания равновесия их массы требуется большее парциальное давление, чем для плоской поверхности жидкости при заданной температуре. Чем меньше размер частицы аэрозоля, тем больше требуется парциальное давление для поддержания равновесия. Этот эффект называется эффектом Кельвина. Таким образом в случае аэрозолей для достижения пересыщенного состояния требуются более высокие значения коэффициента насыщения. Например, для конденсации капель воды диаметром 0,1 и 0,01 микрона (10-6 м) требуется среда с коэффициентом насыщения более 1,022 и 1,24 соответственно [4].
Нуклеация бывает двух типов. Частицы могут образовываться при отсутствии конденсационных ядер. Этот процесс, называемый гомогенная нуклеацией, требует больших коэффициентов насыщения, обычно в диапазоне от 2 до 10. Необходимые для этого условия можно создать только в особых лабораторных или химико-технологических процессах. Чистый водяной пар при 20 0С и при коэффициенте насыщения равным 5 спонтанно формирует капли путем однородного зарождения. Это соответствует диаметру Кельвина 2 нм (10-9 м) и означает, что в этом процессе необходимо образование молекулярных кластеров, состоящие примерно из 90 молекул.
Более распространенным механизмом образования частиц аэрозоля является гетерогенная нуклеация. Этот процесс происходит благодаря существующим в воздухе наночастицам, называемыми ядрами конденсации. Они и служат площадками для конденсации. Наша природная атмосфера содержит тысячи этих ядер в каждом кубическом сантиметре воздуха. В пересыщенных условиях наночастицы с увлажняемой поверхностью будет иметь на своей поверхности адсорбированный слой молекул пара. Если диаметр такого ядра больше диаметра Кельвина для определенного условия пересыщения, то пары начинают конденсироваться на его поверхности. Как только начинается конденсация, рост капель продолжается. В качестве ядер конденсации могут выступать и имеющиеся в воздухе капельки с растворенными твердыми веществами (например, морская соль). Растворенные вещества увеличивают скорость роста и уменьшают скорость испарения по сравнению с чистыми жидкостями. Главное, что гетерогенная нуклеация происходит при более низких коэффициентах насыщения, чем однородная. Поэтому мы наблюдаем образование аэрозолей при более низких температурах или давлениях. Так же важно запомнить, чем выше пересыщение в системе, тем больше частиц будет образовываться.
Следующие два важных процесса — конденсация и испарение. Конденсация происходит, когда скорость поступления молекул пара на поверхность частицы аэрозоля больше, чем скорость выхода молекул. Это приводит к росту размера частицы. Испарение является обратным процессом конденсации и приводит к потере молекул и уменьшению частицы. Когда капелька чистой жидкости находится в пересыщенной среде, превышающей требование к коэффициенту насыщения, заданное уравнением Кельвина, капелька вырастает за счет конденсации паров на ее поверхности. Скорость роста зависит от коэффициента насыщения и размера частиц. Стоит отметить, что быстрое увеличение размера частиц также приводит к повышению их температуры за счет скрытого выделения тепла во время конденсации. Испарение является противоположностью конденсации и регулируется теми же законами. Испарение будет происходить, когда окружающее парциальное давление паров с учетом эффекта Кельвина меньше, чем давление насыщенных паров (p∞<ps). Итак, чем выше пересыщение в системе, тем больше становятся частицы аэрозоля.
Коагуляция — это процесс роста частиц аэрозолей, возникающий в результате столкновения аэрозольных частиц друг с другом.
Если столкновения являются результатом броуновского движения, процесс называется термической коагуляцией; если они являются результатом движения, вызванного внешними силами, процесс называется кинематической коагуляцией. Термическая коагуляция не требует пересыщения, и является односторонним процессом роста без эквивалентного процесса, соответствующего испарению. Результатом столкновений между частицами является увеличение среднего размера частиц и снижение концентрации аэрозолей.При этом коагуляция является быстрым процессом при высокой концентрации и медленным при низких концентрациях (рис. 5).

Броуновское движение – беспорядочное движение микроскопических видимых взвешенных в жидкости или газе частиц твёрдого вещества, вызываемое тепловым движением частиц жидкости или газа.
Частицы аэрозоля двигаются очень хаотично и легко завлекаются воздушными потоками. Под действием броуновского движения частицы осаждаются на любых поверхностях, с которыми аэрозоли соприкасаются, под действием же седиментации (осаждение частиц под действием гравитации) – лишь на обращенных кверху поверхностях. Поэтому на них всегда гораздо больше пыли, чем на вертикальных стенках. Броуновское движение частиц в аэрозолях тем интенсивнее, чем меньший размер они имеют, и существенно лишь в случае наличия частиц меньше 10-6 м. Под действием воздушных потоков частицы разных размеров имеют разные скорости и за счет этого более быстрые могут сталкиваться с более медленными. Такое явление называется сдвиговой коагуляцией.
Количественные характеристики аэрозолей
В физике аэрозолей существенны лишь две величины — концентрация частиц и их размер. Они определяют все свойства.
Размер частиц является важнейшим параметром, определяющим химический состав, оптические свойства, осаждение частиц и их вдыхание в дыхательные пути человека и многое другое. Так как только конденсационные аэрозоли образуют сферические частицы, чтобы охарактеризовать частицы сложной формы и структуры, вводят большое количество условных параметров, имеющих размерность длины и называемых эквивалентными диаметрами. Кроме того, даже для сферических частиц необходим набор разнообразных эквивалентных диаметров, характеризующих их различные физические свойства. Наиболее употребительными из них являются следующие:
1. Эквивалентный массовый диаметр – диаметр сферы из того же вещества и имеющей ту же массу, что и исходная частица (используется при оценках массовой концентрации аэрозолей). Возможно введение эквивалентного поверхностного диаметра (диаметр сферы из того же вещества и имеющей ту же площадь поверхности, что и исходная частица), полезного при анализе поверхностных свойств аэрозолей;
2. Аэродинамический диаметр – диаметр сферы плотности воды (так как равна 1 г/см3), имеющей ту же скорость смещения относительно газовой среды под действием такой же силы, какую испытывает анализируемая частица (полезен при анализе характеристик движения частиц в газе). Применим для частиц более 0,3 мкм;
3. Стоксовский диаметр – диаметр сферы из того же вещества, имеющей ту же скорость осаждения под действием силы тяжести, что и рассматриваемая частица;
4. Эквивалентный оптический диаметр – диаметр сферы, имеющей то же сечение рассеяния излучения, что и характеризуемая частица (необходим при рассмотрении вопросов оптики аэрозолей).
Эти понятия позволяют считать частицы разной формы, состава одинаковыми, что значительно упрощает расчеты. При этом точность вычислений от экспериментальных данных редко отличается более чем в 1,5 раза.
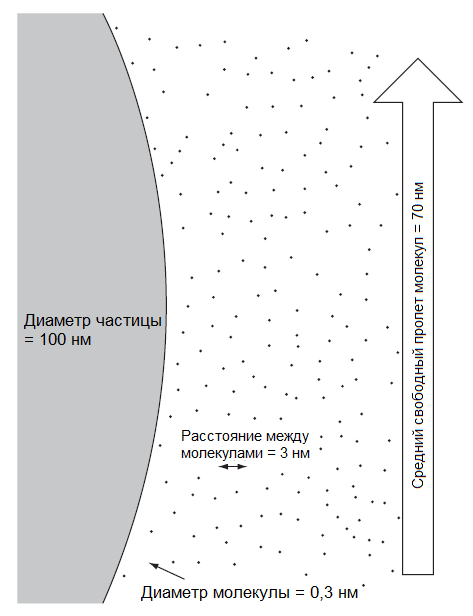
На рис. 7 показаны размеры частиц различных аэрозолей. Они колеблются в широких пределах от 1 нм до 0,1 мм. Минимальный размер частиц определен возможностью существования вещества в агрегатном состоянии. Так, одна молекула воды не может образовать ни газа, ни жидкости, ни твердого тела. Для образования фазы необходимы агрегаты по крайней мере из 20-30 молекул. Самая маленькая частица твердого вещества или жидкости не может иметь размер меньше 1 нм. Чтобы рассматривать газ как непрерывную среду, необходимо, чтобы размеры частиц были гораздо больше, чем свободный пробег молекул газа (см. рис. 6). Верхний предел размеров частиц строго не определен, но частицы крупнее 100 мкм не способны длительное время оставаться взвешенными в воздухе.
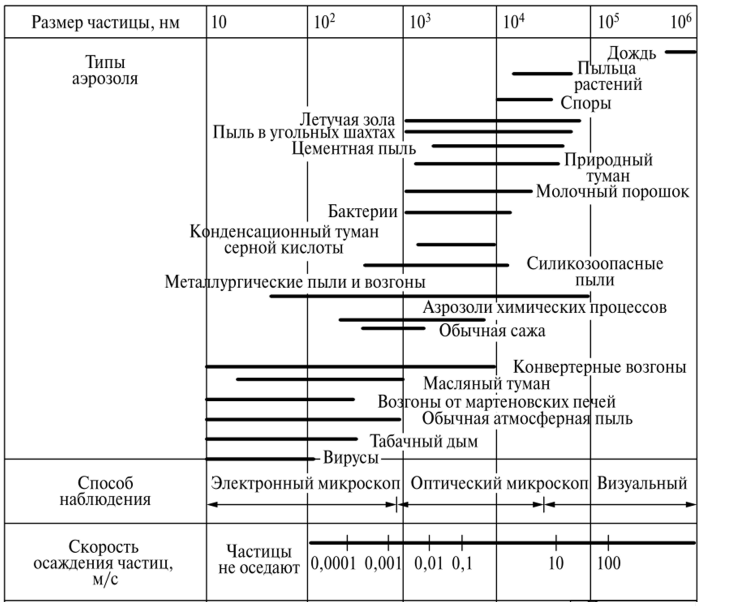
По типу происхождения и по размерам аэрозоли можно разделить на две большие группы: макро- и микрочастицы. Микрочастицы с радиусом меньше 0,5-1,0 мкм образуются в процессах конденсации и коагуляции, тогда как макрочастицы возникают в основном при дезинтеграции поверхности Земли.
Устойчивость частиц так же определяется их размером. Если радиус частиц аэрозоля r > 1 мкм, то iсед » iдиф, т. е. диффузия незначительна, происходит быстрая седиментация и частицы оседают на нижних поверхностях. Если r < 0,01 мкм, то iсед « iдиф, то седиментация незначительна, протекает интенсивная диффузия, в результате которой частицы достигают каких-либо преград и прилипают к ним. Если же частицы сталкиваются между собой, то они слипаются, что приводит к их укрупнению и уменьшению концентрации. Таким образом, из аэрозоля быстро исчезают как очень мелкие, так и очень крупные частицы. Частицы промежуточных размеров обладают максимальной устойчивостью.
Для описания аэрозолей важен не только размер частиц, но и их концентрация. На практике используют массовую и численную концентрации.
Массовая концентрация — масса всех взвешенных частиц в единице объема газа.
Наиболее распространенными единицами массовой концентрации являются мкг/м3. Концентрации массы аэрозолей в атмосфере варьируются от примерно 20 мкг/м3 для чистого воздуха до 200 мкг/м3 для загрязненного воздуха;
концентрации массы в крупных промышленных районах могут составлять несколько мг/м3, а в реакторах промышленных аэрозолей — до 2 г/м3.
Численная концентрация — число частиц в единице объема аэрозоля.
Единицами численной концентрации являются м-3 (или см-3; часто обозначаются как частицы/см3). Общая численная концентрация, включая все размеры, в загрязненной городской атмосфере равна около 105 см-3 или выше, в то время как в менее загрязненных регионах концентрация составляет примерно 104 см-3. Численная концентрация вблизи источников выбросов, таких как выхлопные газы двигателей, или во многих промышленных атмосферах может легко приближаться к 107 см-3 или выше.
Сейчас в научных статьях чаще при исследовании различных аэрозолей определяют величины PM2.5 и PM10.
PM10 – массовая концентрация частиц диаметром менее 10 мкм.
PM2.5 определяется аналогичным образом. Такие границы связаны с возможностью PM2.5 частиц проникать в нижние части дыхательных путей человека, а PM10 задерживаются в верхних дыхательных путях и бронхах.
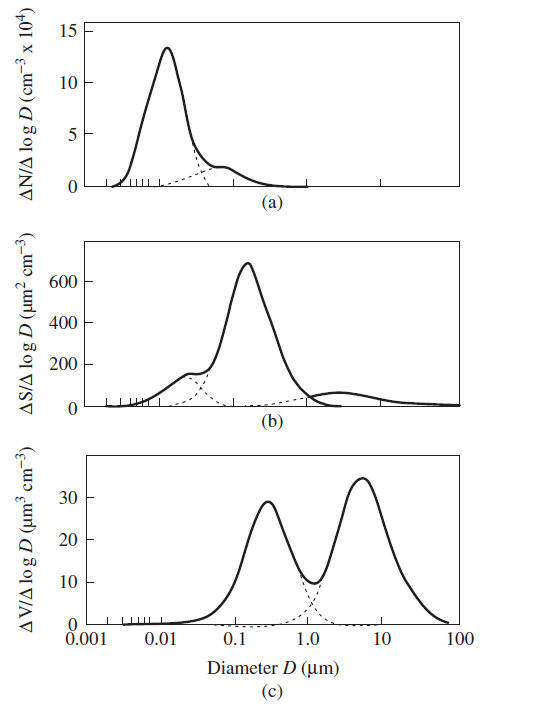
Так как все частицы аэрозоля имеют разные размеры, на практике по полученным экспериментальным данным строят график распределения частиц по размерам. Обычно распределение частиц по размерам является логарифмическим, т.е. концентрация частиц по отношению к размеру частиц выглядит нормальным (также называемым гауссовской кривой), когда размер частиц наносится на логарифмический масштаб. Конденсационные аэрозоли также подчиняются этому распределению. Это доказал в 1954 известный советский метеоролог Л.М. Левин. По данным полученного распределения в качестве представительного размера всех частиц аэрозоля указывается или средний размер (среднее арифметическое всех размеров), или медианный размер (размер, по которому масса всех частиц делится на две равные части.) или модальный (размер соответствующий максимуму плотности распределения вероятности). На рис. 8 показаны графики подобных распределений. В зависимости от используемого типа концентрации получаются разные кривые.
Физические показатели кальянного аэрозоля
Численная концетрация 1,20*106 см-3 . Медианный размер – 0,27 мкм. Менее 0,3 мкм – 62,3 %. 0,3-2,0 мкм — 37%, наночастицы – 19% Условия – саморазжигайющийся уголь, 10 гр Нахлы в чаше, объем затяжки – 500 мл, время затяжки – 1,25 с сессия – 15 мин [7]
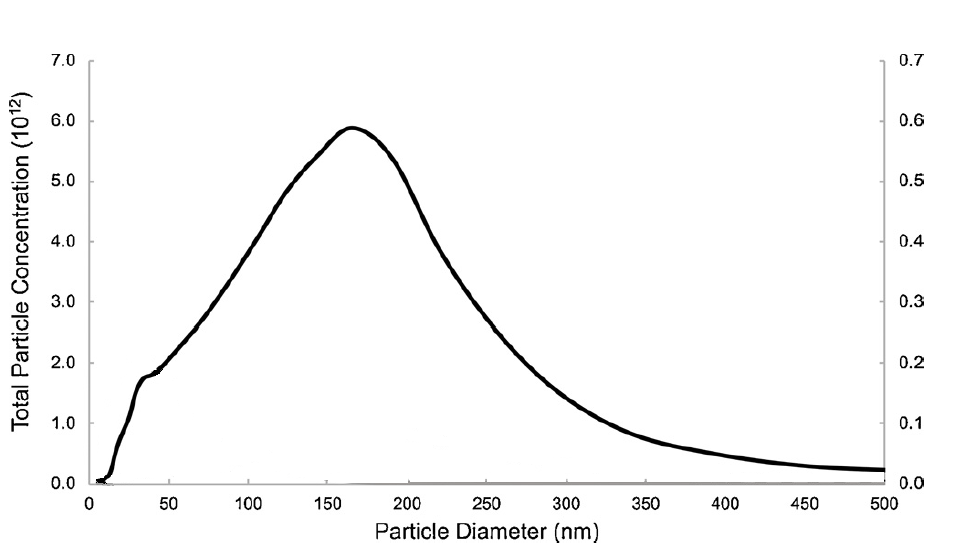
[1] 35-мм Starbuzz Coconut Shell Instant Light charcoal, Для всех испытаний использовалась кальянная трубка Inhale Junior 1 CP (высота трубки 36 см), заполненная дистиллированной водой, объемом 530 мл, сохраняющая 100 мл head space, оснащенная 183-сантиметровым шлангом. Для испытания кальяна использовали 10 г экзотического яблочного американского кальяна Starbuzz® Exotic Apple Americano. Топография затяжек – бейрутский метод. Во время 30-минутного сеанса с кальяном и 35-мм древесным углем образуются частицы числом 6×1013 с диаметром от 5,3 до 530 нм и средним диаметром 130 нм. Массовая концентрация составила – 6 г/м3. Сессия – 30 мин
[8] – 1992 г. исследование. Обнаружены частицы только более 0,52 мкм были обнаружены. Медианный диаметр – 0,8 мкм. Численная концентрация 108 см-3. Данные цифры явно завышены
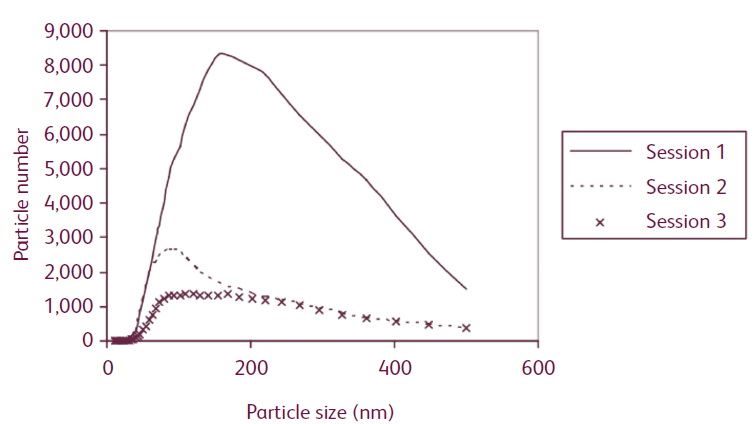
[9] – время затяжки – 3с. Интервал между затяжками – 15 с. Сессия – 30 мин. Обычно средний массовый аэродинамический диаметр (MMAD) для курящих сеансов 1, 2 и 3 составлял 98, 128 и 150 нм. На рисунке 4 показаны средние концентрации частиц во всем диапазоне размеров, измеренные прибором для каждого из трех сеансов курения. Медианная концентрация частиц, составляющая приблизительно 34 000, 13 000 и 9 000 частиц/куб. см, для курящих сеансов 1, 2 и 3 была обнаружена.
[10] —
Литературные источники
[1] — Bernd K, Hauser CD, DeGrood D, et al. Contributions of charcoal, tobacco, and syrup to the toxicity and particle distribution of waterpipe tobacco smoke. Toxicology Letters, 2019
[2] — Pratte P., Cosandey S., and Ginglinger C. Goujon, Investigation of solid particles in the mainstream aerosol of the Tobacco Heating System THS2.2 and mainstream smoke of a 3R4F reference cigarette. Human & Experimental Toxicology, 2017.
[3] — Аэрозоли – дисперсные системы: Монография / Чекман И.С., Сыровая
А.О., Андреева С.В., Макаров В.А. / — Х: «Цифрова друкарня №1», – 2013.
– 100 с.
[4] Aerosol Measurement: Principles, Techniques, and Applications, Third Edition. Edited by P. Kulkarni, P. A. Baron, and K. Willeke, 2011
[5] — Aerosol Science: Technology and Applications, 2014 First Edition. Edited by Ian Colbeck and Mihalis Lazaridis.
[6] — Физика атмосферных аэрозолей: Курс лекций. – Екатеринбург: Изд-во Урал. ун-та, 2008
[7] — Becquemin M.-H., Bertholon J.-F., Attoui M., Roy F., Dautzenberg B., Particle size in water pipe smoke. Revue des Maladies Respiratoires, 2008.
[8] — Haddad A ., Experimental Investigation of Aerosol Dynamics in the Narghile Waterpipe. MS Thesis, Department of Mechanical Engineering, American University of Beirut, 1992.
[9] –Apsley A., Galea K. S., Sánchez-Jiménez A., Assessment of polycyclic aromatic hydrocarbons, carbon monoxide, nicotine, metal contents and particle size distribution of mainstream Shisha smoke. Journal of Environmental Health Research, 2011.
[10] –Perraud V., Lawler M. J., Malecha K. T., Johnson R. M., Chemical characterization of nanoparticles and volatiles present in mainstream hookah smoke. Aerosol Science and Technology, 2019.
[11] — Monzer B., Sepetdjian E., Saliba N., Shihadeh A… Charcoal emissions as a source of CO and carcinogenic PAH in mainstream narghile waterpipe smoke. Food and Chemical Toxicology, 2008